I – COMPOSITION DE L’ACIDE CHLORHYDRIQUE
Expérience 1:
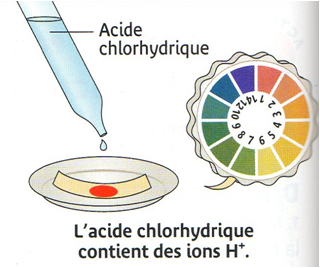
On verse de l’acide chlorhydrique dans un bécher et on mesure son pH.
Observation :
La valeur du pH est égale à 1.
Interprétation :
Le pH de cette solution est acide : cela signifie que l’acide chlorhydrique contient des ions H+.
Expérience 2 :
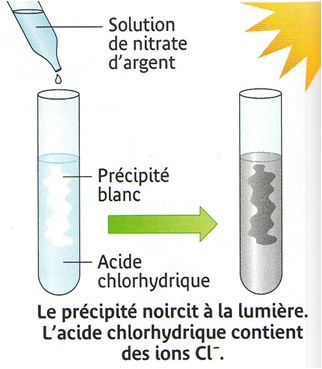
On verse quelques gouttes de solution de nitrate d’argent dans de l’acide chlorhydrique.
Observation :
On observe la formation d’un précipité blanc qui noircit à la lumière.
Interprétation :
Ce précipité prouve la présence d’ions chlorure Cl– dans l’acide chlorhydrique.
CONCLUSION :
L’acide chlorhydrique contient des ions hydrogène H+ et des ions chlorure Cl– en solution dans l’eau.
La formule ionique de l’acide chlorhydrique est ( H+,Cl–).
II – Réaction entre le fer et l’acide chlorhydrique
- Expérience :
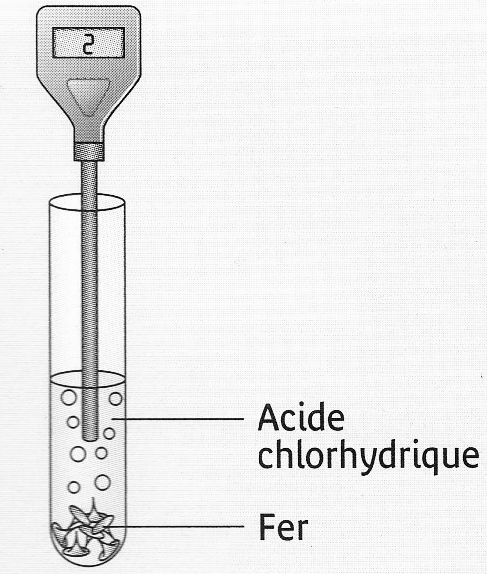
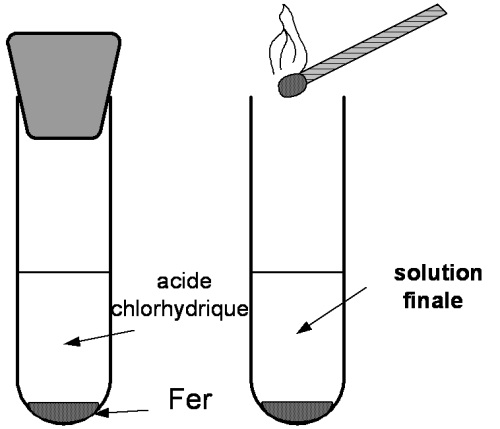
Dans un tube à essais grand modèle, mettre environ 2 pointes de spatule de Fer (Fe) en poudre; puis ajouter environ 5 cm d’acide chlorhydrique et boucher.
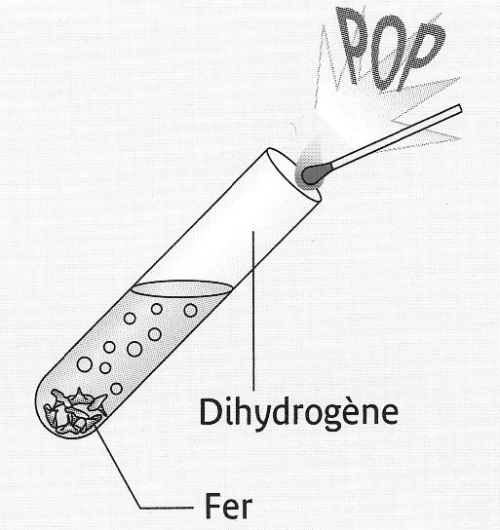
Quand la pression est forte approcher une flamme.
- Observations :
Pendant, la réaction, on observe une vive effervescence.
En présentant la flamme, on entend « un pop » qui caractérise la présence du gaz dihydrogène.
 Interprétation :Une réaction chimique a eu lieu : le fer est un réactif alors que le dihydrogène est un produit.
Interprétation :Une réaction chimique a eu lieu : le fer est un réactif alors que le dihydrogène est un produit.- Analyse de la solution après la réaction :
On récupère la solution après filtration et on réalise deux tests.
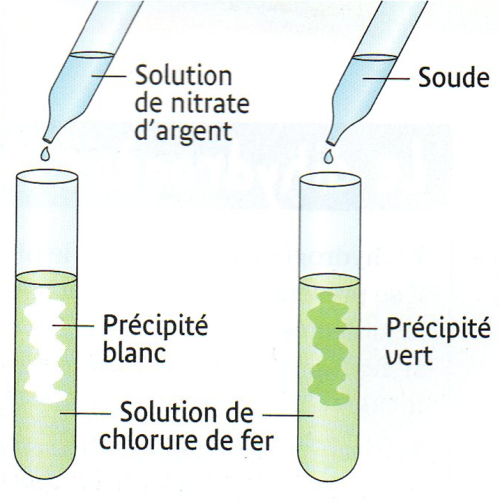
Test à la soude : il se forme un précipité vert qui caractérise la présence d’ions fer II : Fe2+.
Test au nitrate d’argent : il se forme un précipité blanc qui caractérise la présence d’ions chlorure Cl–
Interprétation :
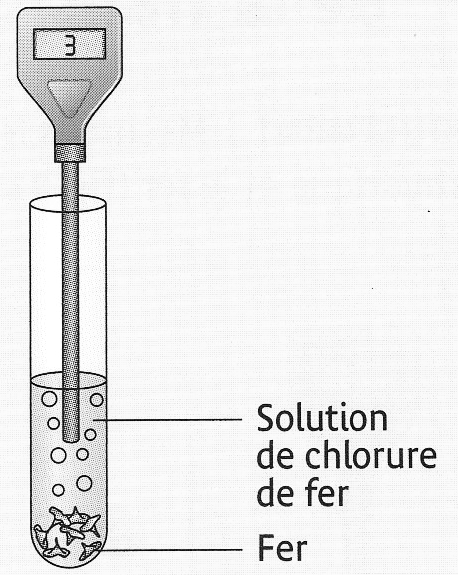
La solution obtenue qui contient des ions chlorure et des ions fer II est une solution de chlorure de fer II.
Conclusion :
On peut écrire le bilan suivant :
Fer + acide chlorhydrique ? dihydrogène + chlorure de fer II
Remarques :
On peut donc écrire un nouveau bilan :
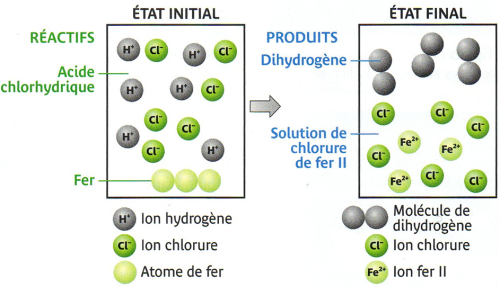
Fer + ions hydrogène ? Dihydrogène + ions fer II
Et l’équation-bilan de la réaction du fer avec l’acide chlorhydrique sera :
Fe + 2H+ ? H2 + Fe2+


Leave a reply
Vous devez vous connecter pour publier un commentaire.