La radioactivité est bien loin en ces périodes de révisions et une petite fiche pour explorer les connaissances exigibles en radioactivité ne peut pas faire de mal.
Connaître la signification du symbole ZAX et donner la composition du noyau correspondant.
Voici une vieille connaissance qui date de la seconde :
ZAX : noyau de symbole X qui a pour nombre de masse A et numéro atomique Z. Un noyau ZAX est donc constitué de Z protons et A-Z neutrons.
Définir l’isotopie et reconnaître des isotopes.
2 noyaux isotopes ont le même nombre de protons mais un nombre différent de neutrons. Ainsi, ils ont le même Z mais pas le même A.
Reconnaître les domaines de stabilité et d’instabilité des noyaux sur un diagramme (N,Z).
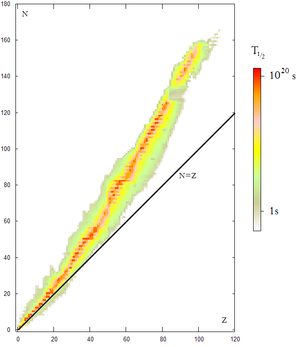
Il s’agit de reconnaitre sur un diagramme du type :
Qu’il y a une zone correspondant à des noyaux stable, donc non radioactifs. Sur le diagramme ci-dessus, c’est la zone la plus rouge. On voit que pour des petits Z, cette zone suit plus ou moins la courbe N=Z, puis s’en éloigne au fur et à mesure que les Z devient de plus en plus grand.
Et qu’autour de cette zone, les noyaux sont de plus en plus instables au fur et à mesure qu’on s’en éloigne. Le reste du diagramme (en blanc ici) correspond à des noyaux qui ont une durée de vie tellement infinitésimale qu’il n’a jamais été possible de les fabriquer.
Définir un noyau radioactif.
Un noyau radioactif est un noyau qui subit spontanément une désintégration nucléaire. Cela se traduit par l’émission d’un rayonnement et la transmutation du noyau père en un noyau fils.
Connaître et utiliser les lois de conservation.
Lors d’une désintégration nucléaire, le nombre total de nucléons et le nombre de charge se conservent. Ce sont les lois de Soddy. Ainsi, lors d’une désintégration ? qui produit un noyau d’Hélium (A=4 et Z=2), on aura :
![]()
Par exemple, un noyau d’uranium 238 (A=92, Z=92) se désintègre en Thorium 234 (A=234 et Z=90).
Définir la radioactivité ?, ?+?, ?– l’émission ? et écrire l’équation d’une réaction nucléaire pour une émission ?, ?+?, ?–? en appliquant les lois de conservation.
- La radioactivité ? se caractérise par l’émission d’un noyau d’hélium He : A=4, Z=2.
- La radioactivité ?+? se caractérise par l’émission d’un positron : un anti-électron qui porte à les mêmes caractéristiques qu’un électron si ce n’est sa charge qui est positive et A=0 (il ne s’agit pas d’un nucléon) et Z=1 (charge positive).
- La radioactivité ?–? se caractérise par l’émission d’un électron : A=0 (il ne s’agit pas d’un nucléon) et Z=-1 (charge négative).
- L’émission ? correspond à la désexcitation du noyau fils. En effet, une désintégration radioactive produit beaucoup d’énergie et le noyau fils est bien souvent dans un état excité (voirs le cours de fin d’année sur la quantification des niveaux d’énergie). Le passage de l’état excité à l’état au repos passe par l’émission d’un rayonnement électromagnétique nommé rayonnement ?.
Ainsi, un noyau Cobalt 60 (symbole Co, A=60 et Z=27) radioactif ?– produira un électron (A=0, Z=-1) et son noyau fils sera carctérisé par (A=60 et Z=28) pour assurer les lois de conservation de Soddy. Si l’on regarde dans un tableau périodique des éléments, on trouvera que Z=28 correspond au Nickel (symbole Ni). L’équation de désintégration s’écrit donc :
6027Co ? 6028Ni + 0-1e
À partir de l’équation d’une réaction nucléaire, reconnaître le type de radioactivité.
Celle-ci est assez simple, il suffit de reconnaître l’élément éjecté : une noyau 42He c’est de la radioactivité ?, un positron 01e c’est du ?+ et un électron 0-1e c’est du ?–. Attention la présence d’un noyau d’hélium dans les produits ne signifie pas obligatoirement qu’on a affaire à une radioactivité ?. Il est possible également que ce soit une réaction de fusion. Besoin de se rafraîchir la mémoire ? Jetez donc un oeil sur la fiche Réaction nucléaire.
Connaître l’expression de la loi de décroissance et exploiter la courbe de décroissance.
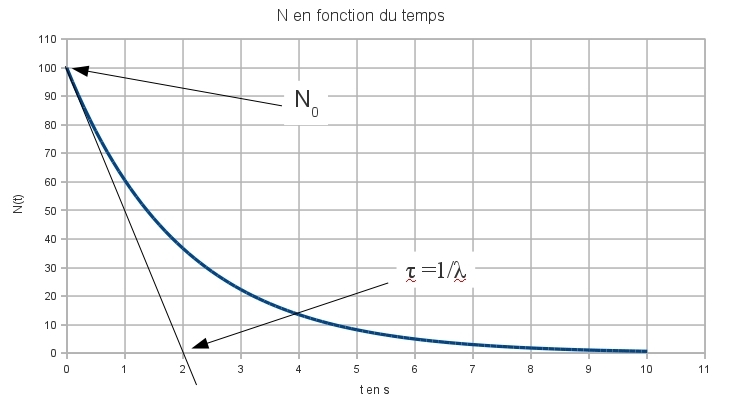
Une population de noyau décroit en suivant la loi de décroissance suivante : N(t)=N0e-?t. Cela se traduit par :
Sur le graphique, on trouvera comment lire la valeur de N0 et comment trouver ?.
Savoir que 1 Bq est égal à une désintégration par seconde.
Dit comme ça c’est un peu rapide. Déjà il faut savoir que le Becquerel, Bq, (du nom d’un physicien qui a compté… on fait comme ça en physique : on donne le nom des gens qui comptent à des unités comme ça on est sûr que les apprentis retiendront leur nom même s’ils ne savent pas de qui il s’agit) est l’unité de l’activité d’une source radioactive. Et donc, lorsque pour une source radioactive il y a une désintégration par seconde, alors son activité est de 1 Bq. Ainsi le Bq est égal à des s-1.
Pour info : 1 Bq c’est tout petit, une source radioactive qui émet une particule par seconde, c’est à peine détectable. Dans un exercice où l’on vous fait calculer l’activité d’une source radioactive, ne vous étonnez pas de trouver de très grand nombre. Avant le Bq, on utilisait le Ci (de Curie) qui vaut 3,7·1010 Bq. C’est une unité plus adaptée à la radioactivité mais elle n’est pas « standard ».
Expliquer la signification et l’importance de l’activité dans le cadre des effets biologiques.
Une source radioactive émet des radiations très énergétique. lorsque ces radiations arrivent sur un organisme vivant, c’est comme un éléphant dans un magasin de porcelaine : ça fait beaucoup de dégat (voir les effets biologiques de la radioactivité I & II). Ainsi, l’activité qui mesure le nombre de désintégration par seconde donne une bonne idée de la dangerosité d’une source. Plus elle est active, plus elle est susceptible d’avoir un impact biologique.
Connaître la définition de la constante de temps et du temps de demi-vie.
La constante de temps est l’inverse de la constante radioactive ? qui apparaît dans l’expression de la loi de décroissance radioactive : N(t)=N0e-?t. ?=1/?.
Le temps de demi-vie est la durée pour qu’une population de noyau soit divisée par 2 : N(t1/2)=N0/2.
Utiliser les relations entre ? et ? et t1/2.
Noter bien qu’il est dit « utiliser » et pas « savoir les démontrer », donc à priori, il n’est pas nécessaire de savoir démontrer que N(t1/2)=N0/2 implique que t1/2=ln2/?. Cependant, ce calcul est parfois demandé (voir par exemple Liban 2008 sur labolycee.org). Pour mémoire :
N(t1/2)=N0/2 ? N0e-?t1/2 = N0/2 ? e-?t1/2 = 1/2 ? e?t1/2 = 2 ? ?.t1/2=ln2
D’où t1/2=ln2/? et en se rappelant que ?=1/? on peut écrire : t1/2=?.ln2.
Pour l’application de ces expressions, attention aux unités : si ? est en seconde, alors t1/2 l’est aussi. Cependant t1/2 est souvent donner en heure ou en seconde, donc il faut le convertir en seconde pour avoir ? en seconde et ? en s-1.
Ceci est extrêmement important car l’activité (nombre de désintégration par seconde) est égale à la dérivée de N par rapport au temps : A=-dN/dt qui est égal à ?N. Ainsi l’unité de ? donne l’unité de A. Comme A est en Bq (donc en s-1) alors, il faut toujours exprimer ? en s-1.
Un exemple ? Envisageons une source de carbone 14 contenant 1 mole de noyaux (6.1023 noyaux). La demi-vie du carbone 14 est de 5 730 ans. Ainsi, ?=ln2/t1/2=ln2/t1/2=ln2/(5730*365*24*3600)=3,84 10-12 s-1 et A=2,3 1012 Bq.
Déterminer l’unité de ? ou de ? par analyse dimensionnelle.
Celle-ci est assez facile : Sachant que ln2 est juste un nombre sans unité, t1/2=ln2/? implique que t1/2 et ? ont une unité inverse l’une de l’autre. Si t1/2 est en heure alors ? est en h-1. Pour ?, t1/2=?.ln2 implique que t1/2 et ? ont la même unité.
Expliquer le principe de la datation, le choix du radioélément et dater un événement.
Du fait de la décroissance exponentielle d’une population de noyaux radioactive, une source a une activité qui décroit de manière exponentielle : A(t)=A0e-?t. Ainsi, connaissant le temps de demi-vie de l’élément considéré et l’activité initiale, il est facile de trouver l’age de l’échantillon en mesurant son activité à l’instant présent.
Bien entendu, connaître l’activité initiale n’est pas facile. Il faut faire des raisonnements très rusé pour y arriver. Cependant, dans tous les sujets de bac traitant de datation on vous guide tout au long du raisonnement qui permet de déterminer l’activité initiale.
Un exemple classique de datation : la datation au carbone 14. Elle est basée sur le fait que le carbone 14 (isotope radioactif du carbone) est continuement régénéré dans la haute atmosphère. Ainsi le taux carbone 14 sur carbone 12 (C14/C12) est constant dans l’atmosphère, de l’ordre de 10-12. Comme les plantes « respirent » le carbone de l’air (par le dioxyde de carbone), le taux C14/C12 des plantes est le même que celui de l’atmosphère. A partir du moment où l’organisme vivant meurt, les échanges cessent et la quantité de Carbone 14 décroit de manière exponentielle. Ainsi, une mesure de l’activité radioactive due au carbone 14 permet de savoir depuis combien de temps l’organisme est mort. Le temps de demi-vie du carbone 14 étant de 5730 ans, on peut pas remonter plus loin que 50 000 ans. Au-delà de cette durée, il n’y a plus assez de Carbone 14 pour mesurer l’activité radioactive.
slt prof q’est-ce qu’il retenir en grosomodo sur ce cour.
slt eleve, tout ce qui est noté en gras dans cet article, pas moins.