En TS, vous voilà perdu avec les spectres RMN ? Pas de panique, voyons un peu ce qu’il faudra en retenir :
Je sais relier un spectre RMN simple à une molécule organique donnée, à l’aide de tables de données ou de logiciels.
Je sais identifier les protons équivalents et relier la multiplicité du signal au nombre de voisins.
Grande nouveauté du Bac 2013, la spectroscopie RMN sera donc surtout utilisée dans les sujets pour déterminer si un échantillon contient une molécule de formule donnée. Voyons un peu de quoi il s’agit.

RMN signifie Resonance Magnétique Nucléaire. Le principe consiste à soumettre un échantillon à un très fort champ magnétique ce qui permet d’aligner le spin des noyaux d’atome d’hydrogène. Ce champ est produit par des supraconducteurs. Cette technique est donc coûteuse et « massive ».
En « titillant » ces noyaux à l’aide d’un champ magnétique perpendiculaire au premier et ayant la bonne fréquence, ceux-ci vont réagir en produisant un signal qui sera analysé par un ordinateur :
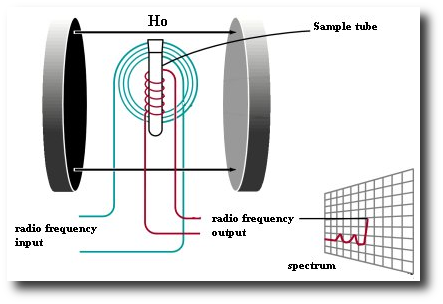
C’est un peu comme si en tapant sur les noyaux d’hydrogène et en analysant leur réponse, ceux-ci nous donnait des informations sur leur environnement. La méthode fait penser aux cheminots de l’ancien temps qui frappaient les roues des wagon pour vérifier que tout allait bien. Pour comprendre comment fonctionne la RMN, on peut voir cette animation java, expliquée ici (en anglais avec un accent danois).
Cette méthode n’est pas qu’utilisée en chimie, elle permet d’obtenir de beaux clichés de l’intérieur du corps sans avoir à l’ouvrir (ce qui est assez pratique vous en conviendrez). En médecine, on n’appelle pas ça la RMN mais IRM. On a remplacé le N de nucléaire par le I de imagerie. C’est exactement la même chose mais ça fait un peu moins peur aux patients…
Pour le bac, il faut être capable d’interpréter un spectre RMN. Il n’est pas demandé de comprendre le principe, je ne m’étendrais donc pas sur ce sujet. Un spectre RMN en chimie ressemble à ça :
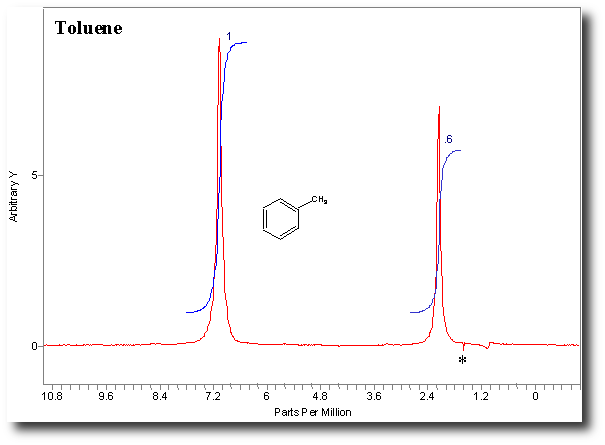
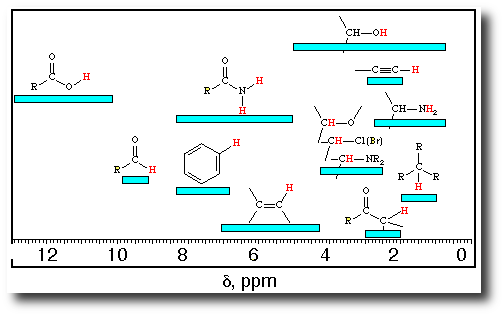
En abscisse, c’est le déplacement chimique. On n’a pas besoin, en terminale, de savoir à quoi ça correspond. Il faut juste retenir que le zéro est à droite (oui, je sais encore une bizarrerie, comme pour les spectres IR) et que s’il y a un pic en zéro on ne s’en occupe pas. Ce qu’il va falloir analyser ce sont les autres pics. Ceux-ci correspondent à certains noyaux d’atomes d’hydrogène de la molécule. Leur position dans le spectre nous renseigne sur le groupe d’atomes, donc la fonction :
Comme un noyau d’hydrogène est simplement un proton, on parle plutôt de protons en RMN que d’hydrogène. Sur le spectre du toluène ci-dessus, on remarque 2 pics alors que la molécule présente 8 protons (3 sur le groupe méthyl et 5 sur le cycle aromatique). Ceci vient du fait que des protons équivalents résonnent de la même façon. Voici une première règle qu’il va falloir retenir :
Dans un spectre RMN, les protons équivalents, c’est à dire ceux qui ont le même environnement chimique, ont la même valeur de déplacement chimique
Ainsi, les protons sont tous cachés dans les pics et il ne suffit pas d’identifier un pic pour savoir à combien de protons il correspond. Pour résoudre cette énigme, les chimistes utilisent la courbe d’intégration. Kézako que ce truc ? Il s’agit d’une courbe qui en x prend comme valeur la somme de toutes les valeurs du spectre précédant x. Dans notre cas où le spectre est une suite de pics, la courbe d’intégration est nulle avant le premier pic puis garde la valeur du premier pic jusqu’au second, etc. Elle forme donc un palier comme on peut le voir ci-dessous :
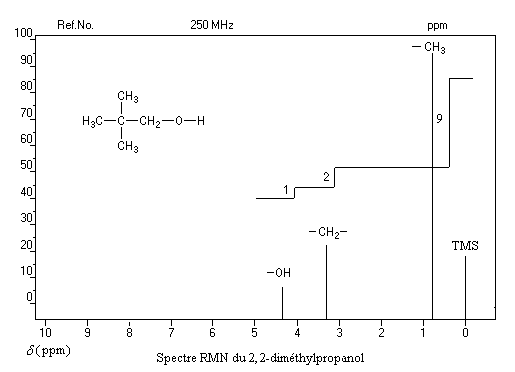
La « hauteur de marche » correspond donc au nombre de protons qui se cachent dans le pic. Ici, il y a 1 proton dans la fonction alcool, 2 dans CH2 et 9 dans des groupements méthyl CH3. On pourra s’amuser avec les spectres présentés dans le paragraphe Signal strength de cette page. En cliquant sur les pics, on voit apparaître les courbes d’intégration correspondantes.
Si les choses pouvaient s’arrêter là, ce serait bien mais il y a encore une petite chose qu’il faut connaître à propos des spectres RMN : la notion de multiplicité du signal. Sur le spectre de l’éthanol ci-dessous,
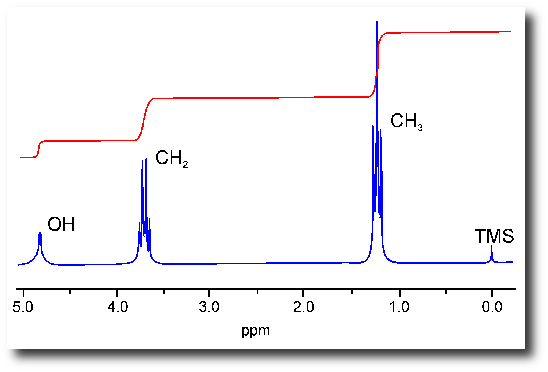
on observe que les pics sont constitués en fait de plusieurs pics : un singulet (un seul pic) puis un quadruplet (4 pics) et enfin un triplet (3 pics). Cela vient de l’influence des différents protons les uns sur les autres. Prenons le quadruplet du milieu. Il est due aux deux protons rattachés au carbone du milieu (HO-CH2-CH3). Pourquoi n’observe-t-on pas simplement un grand pics ? Tout simplement parce que les protons portés par les carbones voisins ont une influence sur ces deux protons. Ainsi, les 3 protons qui sont portés par le carbone du groupement méthyl (HO-CH2-CH3) vont éclater ce pic en 4 pics. Pour ces protons qui « voient » les 2 protons du milieu, le pic est éclaté en 3 pics. C’est la règle des (n+1)-uplet :
un proton ou un groupe de protons équivalents ayant n protons voisins équivalents donne un signal constitué de (n+1) pics.
Quand on dit voisins, on veut dire portés par un carbone voisin de celui qui porte le proton considéré. Ok, mais alors pourquoi le proton porté par l’oxygène de la fonction alcool (HO-CH2-CH3) n’est pas un 2+1-uplet, c’est à dire un triplet ? Il a bien 2 protons voisins, non ? Oui, ils semblent avoir deux voisins… mais non car
les protons des groupes OH, COOH et NH ne peuvent se coupler avec les autres.
C’est bizarre ce truc. Oui mais c’est comme ça. Et il va falloir le retenir.
Ouf ! Nous avonc vu tout ce qu’il faut retenir pour traiter les spectres RMN pour le bac 2013. Il va falloir maintenant mettre tout ça en pratique avec des exercices. Il ne vous sera pas demandé de trouver la formule d’une molécule inconnue à partir d’un spectre RMN, c’est bien trop compliqué mais de relier une molécule à son spectre RMN. Comment faire ? Voici la méthode :
- Repérer les protons équivalents
- Repérer les groupes de signaux du spectre
- Utiliser les sauts de la courbe d’intégration pour faire le lien entre le spectre et la molécule
- Exploiter la multiplicité des signaux pour confirmer ou corriger l’attribution des signaux
- Exploiter une table de donnée
Bon courage !
One thought on “La spectroscopie RMN”